凭“空“制造:利用空气基二氧化碳高效合成氨基酸和有机酸
合成生物学作为第三次生命科学革命正与生物制造携手推动新一轮产业革命:据估计,未来生物制造有望占据全球制造业市场规模的1/3,达到30万亿美元。以淀粉及糖为主要原料的传统生物制造无法满足这一未来发展的需要,存在着“与民争粮”的风险和不可持续性。另一方面,因气候变化,二氧化碳的捕捉和资源化利用在全球受到极大的关注,空气基CO2为生物制造提供了前所未有的机遇与挑战。CO2是取之不尽、用之不竭的碳资源,其利用是“双碳目标”的必经之路,然而,在生物合成意义上CO2的有机能量为零。能量输入是CO2利用的核心科学问题,其形式极大地决定了固碳的效率和速率,而后者是生物制造的技术关键。天然CO2利用途径如光合作用的速率远远达不到生物制造的需求。近年来,人们开发了不同的人工生物固碳途径,包括间接地利用由CO2衍生的一碳化合物(C1),如甲醇、甲酸或甲醛等作为原料。但是C1原料的生物利用普遍存在着以下挑战:大多需要消耗昂贵的能量辅因子ATP和还原力辅因子NAD(P)H;所需酶的数量和种类往往较多,导致多酶体系协同性和路径鲁棒性较差,在胞内应用时尤为突出;固碳速率受限于途径的热力学(能量输入)和生物体系固有的动力学推动力不足。
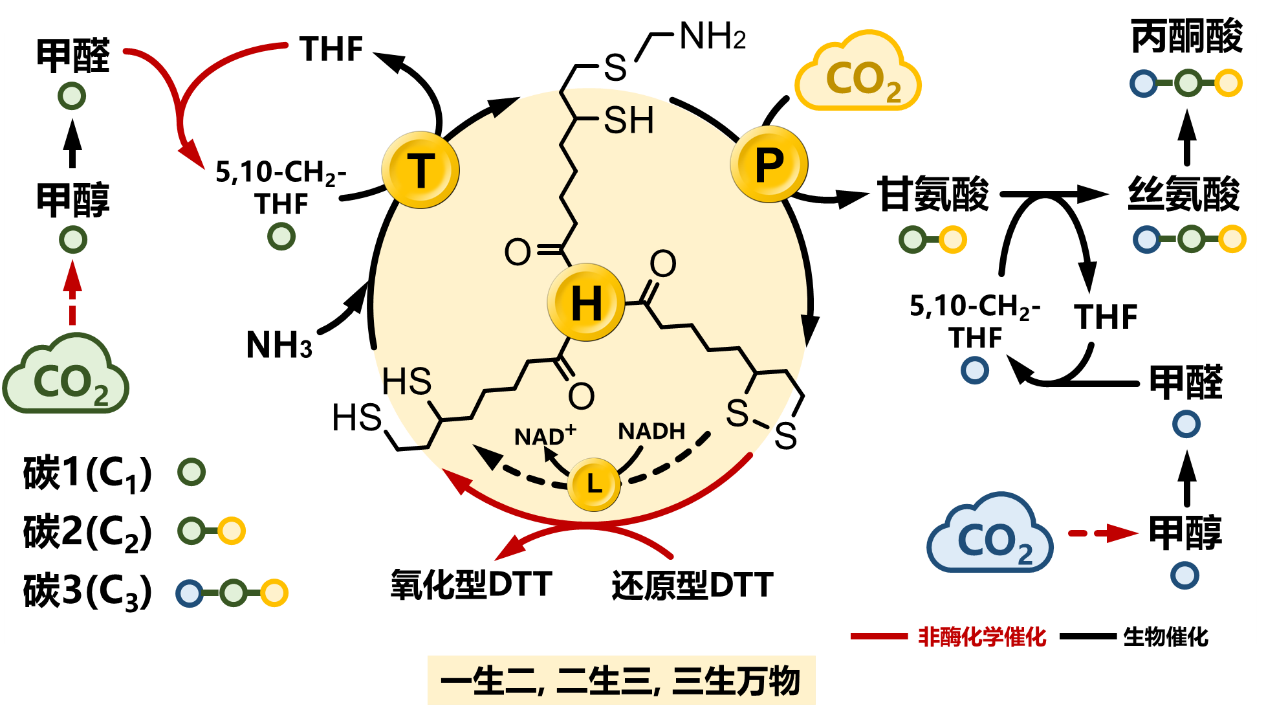
图1. 生物催化与化学催化(非酶)有机整合的固碳路线ICE-CAP
针对上述挑战,西湖大学曾安平教授团队创建了一条全新的细胞外化学催化与生物催化有机整合的高效固碳路线(ICE-CAP: Integrated Chemoenzymatic CO2 to Amino-acid Pathway)和工艺过程(图1)。通过高能C1化合物(甲醇或甲醛)与低能C1化合物(二氧化碳)的化学生物巧妙组合催化,成功实现了不需要添加能量辅因子ATP和还原力辅因子NAD(P)H的CO2生物利用。 通过过程集成,实现从甲醇和由空气中捕捉的CO2高效合成甘氨酸(C2),丝氨酸(C3)和丙酮酸(C3),产品浓度均达到g/L的水平。这项工作最近发表在Nature communications上,受到评审人的高度赞赏,指出这是体外生物合成这一新兴领域中的一个巧妙案例,展示了化学-酶催化的能力(“It represents an elegant example in the emerging field of in vitro biosynthesis and underlines the capability of chemoenzymatic processes.”)。
ICE-CAP实现了迄今为止最高的生物固碳速率(67.8 nmol C1/min/mg蛋白),比已有文献报道的固碳速率提高2-10倍,突破了近年来倍受关注的以甲酸及CO2为原料的还原性甘氨酸途径的极低合成速率。它为一碳化合物的利用提供了一条全新的“一生二,二生三,三生万物”的生物代谢途径。其具体特征包括:
1.化学催化与生物催化有机整合,克服固碳途径热力学能量限制
ICE-CAP的核心模块是甘氨酸裂解体系(GCS, glycine cleavage system),逆转“甘氨酸裂解体系”成为“甘氨酸合成体系”是文章的突破之一。GCS由氨基转移酶T蛋白,羧化酶P蛋白,二氢硫辛酰胺脱氢酶L蛋白和穿梭蛋白H组成。本研究发现二硫苏糖醇DTT介导的硫还原化学反应可以取代电子供体NADH和相应的L蛋白,用于再生还原型的H蛋白,而且有更为优越的热力学推动力 (图2)。在DTT存在的条件下,甘氨酸合成速率相比于在NADH条件下有明显的提高。本工作建立的第二个自发化学反应,即甲醛与四氢叶酸(THF)的缩聚,将GCS体系与甲醇利用有机整合,突破了传统还原甘氨酸途径依赖甲酸的局限性,进一步提高了ICE-CAP的效率和可行性。

图2. 利用化学还原剂替代NADH的甘氨酸合成体系实现了化学催化和生物催化的有机整合
2. 一石二鸟: DTT阻止羧化酶P蛋白的自聚集从而提高羧化效率
甘氨酸脱羧酶P蛋白是固碳的核心,其活性中心内部二硫键的形成(Cys335-Cys949)及C端Loop区域的空间位置会极大地影响酶的活性,而且P蛋白在胞外容易形成多聚物 (图3)。巧妙的是,在DTT存在的条件下,一方面会通过还原打开P蛋白分子内部的二硫键,便于羧化酶的辅因子进入P蛋白活性中心发挥活性;另一方面会极大程度地抑制P蛋白多聚物的形成,将P蛋白维持在高活性状态。
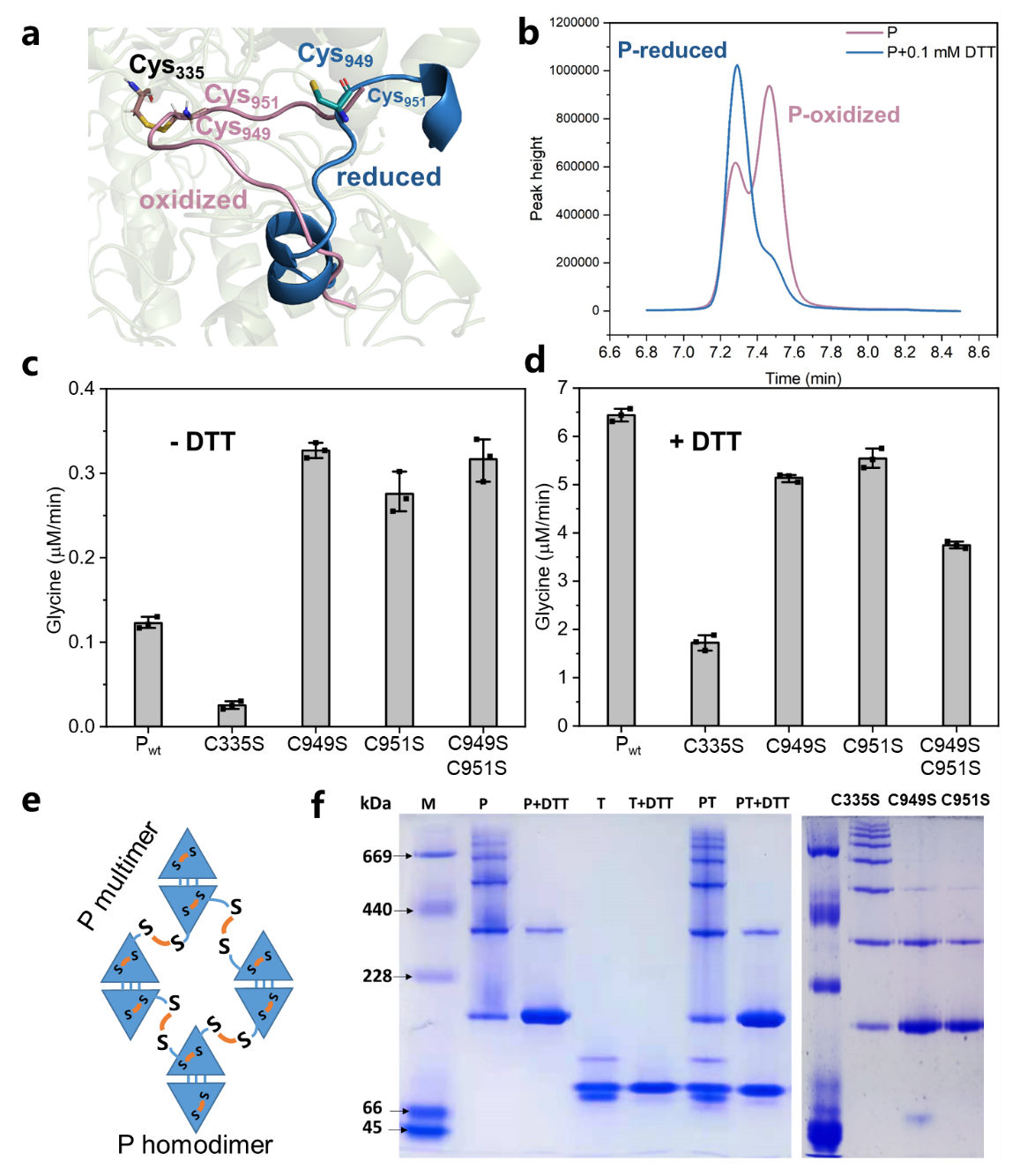
图3. DTT还原羧化酶P蛋白的二硫键并阻止其自聚集从而提高羧化效率
3. 三管齐下:破坏H蛋白的自我保护机制提高固碳效率
在前面两个突破的基础上, 作者进一步通过分子动力学模拟研究了硫辛酰胺臂在H蛋白空腔的分子运动轨迹,鉴定了关键的氨基酸位点及其突变对固碳速率的影响(图4)。以Y70A H蛋白突变体为例,由于破坏了H蛋白的自我保护机制,硫辛酰胺臂更容易暴露在H蛋白空腔的外部,从而更有利于后续和P蛋白结合进行固碳反应,甘氨酸合成速率进一步地提高两倍。
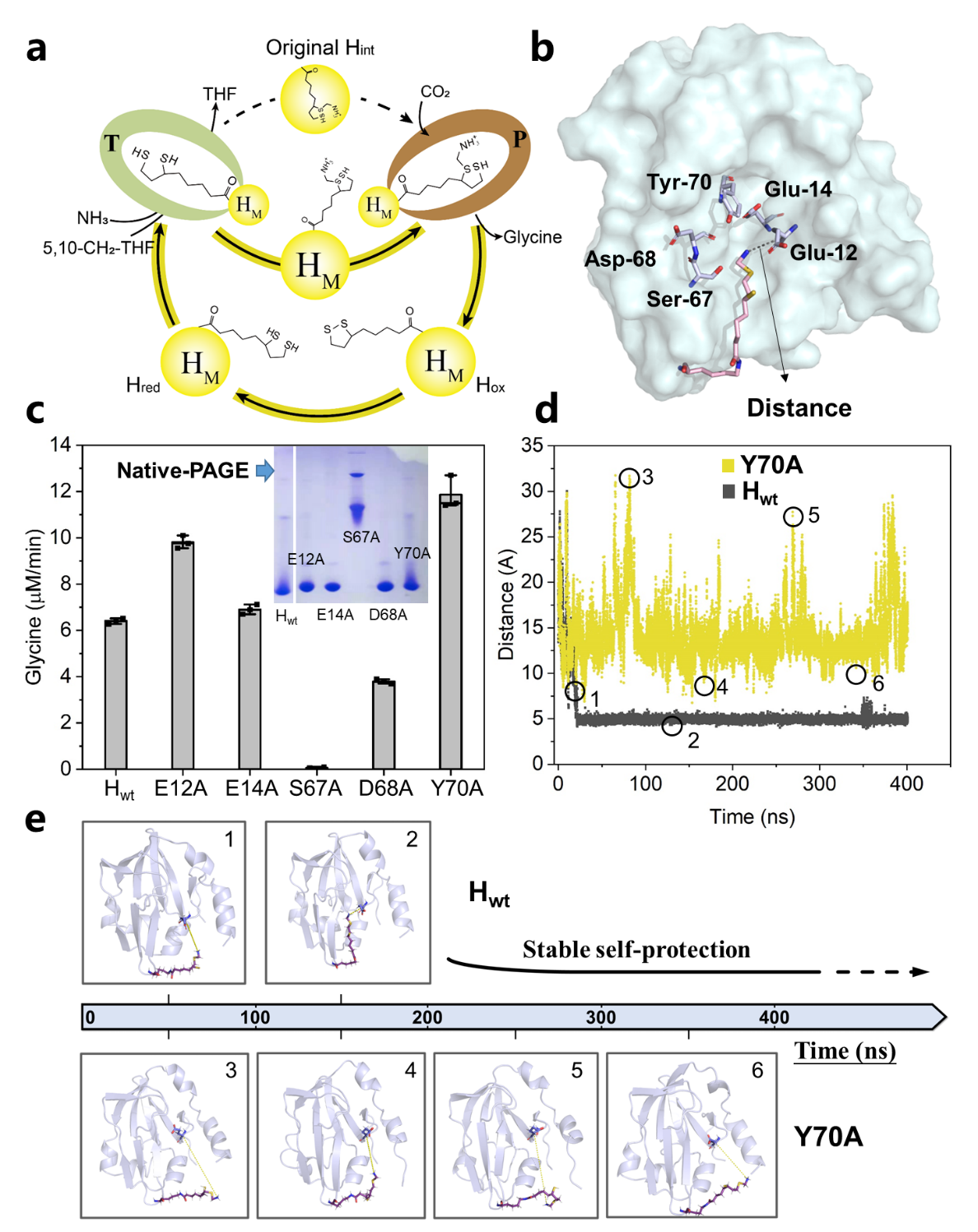
图4. 通过结构指导的蛋白质改造破坏H蛋白的自我保护机制提高羧化效率
4. 直接利用气态二氧化碳生产氨基酸
在揭示了DTT在甘氨酸合成体系的作用机和H蛋白催化机制的基础上,作者组装了一个高效的固碳分子机器,以甲醛和二氧化碳为底物实现了1.2 g/L的甘氨酸的合成 (图5)。该体系也适用于对含高浓度二氧化碳的发电厂、钢铁厂等工厂废气的无缝连接使用。
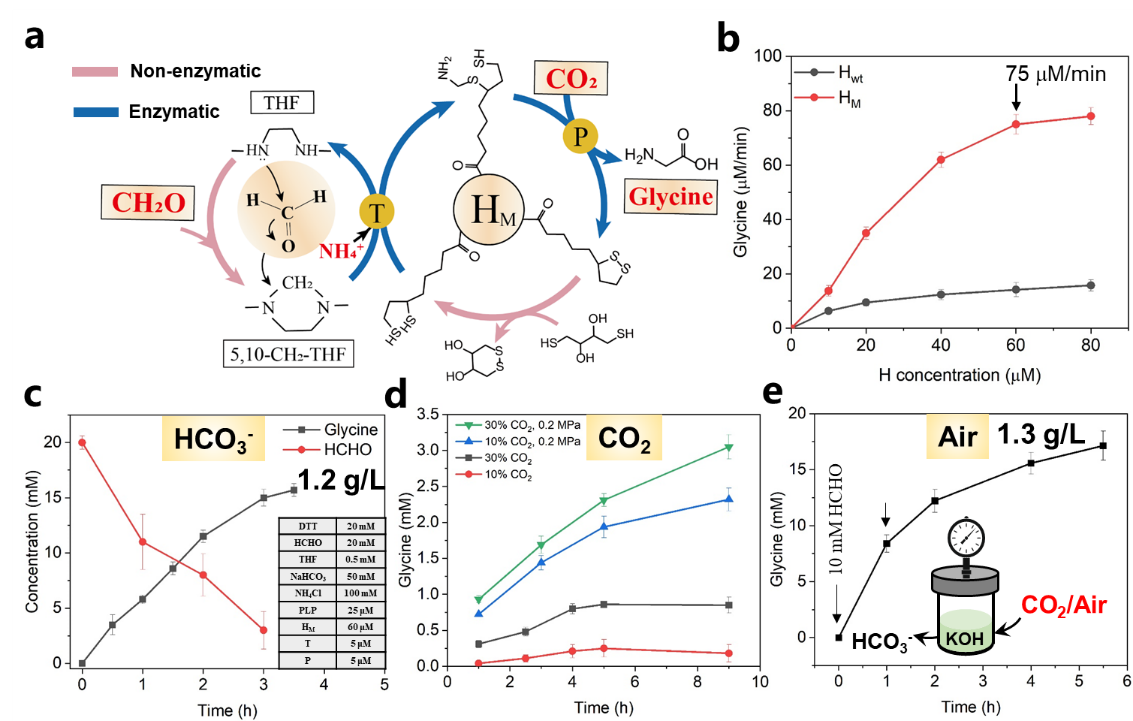
图5. 直接利用气态二氧化碳生产氨基酸
5. 利用空气中捕捉的二氧化碳生产氨基酸
利用甲醇和从空气中捕捉的二氧化碳,作者分别实现了g/L级别的甘氨酸,丝氨酸和丙酮酸的高效合成(图6)。
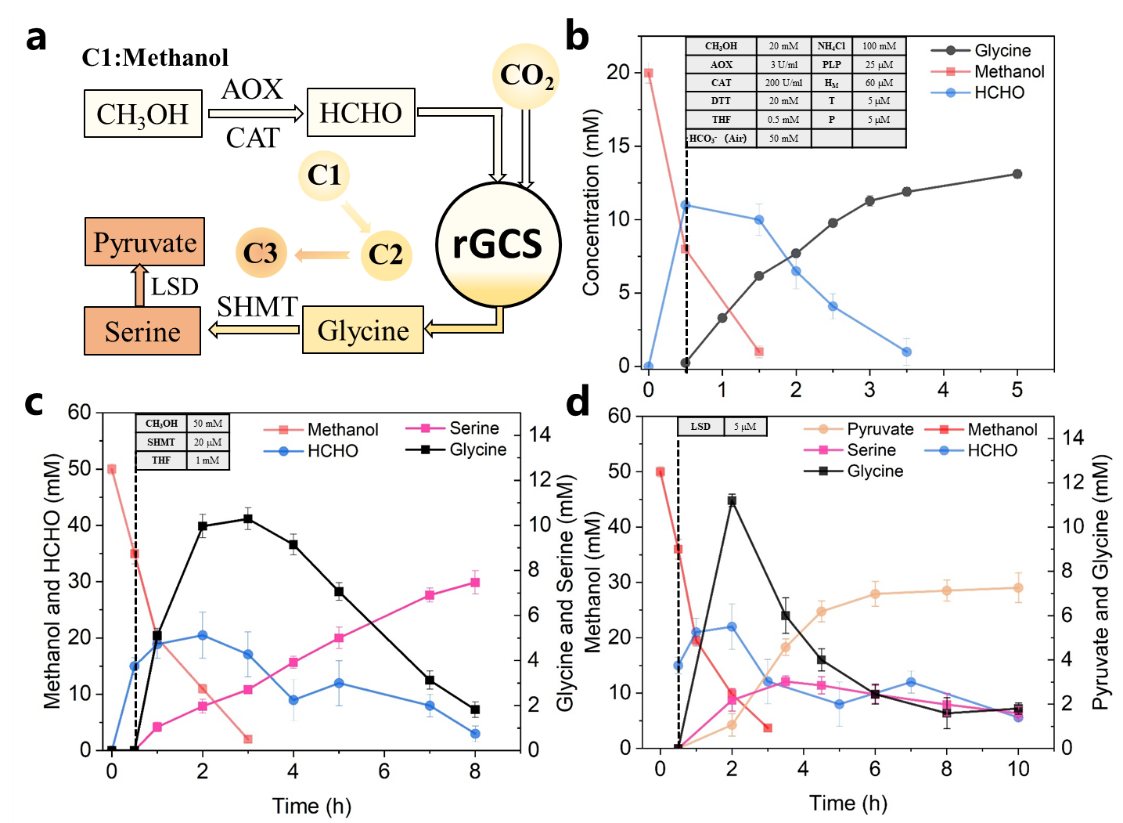
图6 空气中捕捉的二氧化碳和甲醇耦合反应生产氨基酸和丙酮酸
该工作展现了生物催化和化学催化结合的巨大潜力,实现了利用气相及空气中的二氧化碳(一碳)高效合成氨基酸(二碳或三碳)及丙酮酸(三碳)。从二氧化碳生物合成高附加值化学品是双碳目标及合成生物学的重要方向,目前所报道的方法通常是基于液态的一碳化合物(碳酸氢根等),并且需要昂贵的能量辅因子ATP和还原力辅因子NADH。曾安平团队创建了全新的化学法与生物法有机整合气相二氧化碳和高能C1(甲醇或甲醛)共固碳路线,实现了国际上唯一的不需要消耗ATP和NADH的新型低碳制造模式。该方法突破了二氧化碳生物转化的热力学能量限制,达到了迄今为止最高的二氧化碳固碳效率,为创造基于二氧化碳的“一生二,二生三,三生万物”的颠覆性生物制造技术奠定了坚实的基础。

